【骨鬆Q&A 011】什麼是AVA(Anabolism Vs Antiresorption)trial ?
Anabolism Vs Anti-resorption
造骨促進 破骨抑制


Differential Effects of Teriparatide and Denosumab on Intact PTH and Bone Formation Indices: AVA Osteoporosis Study
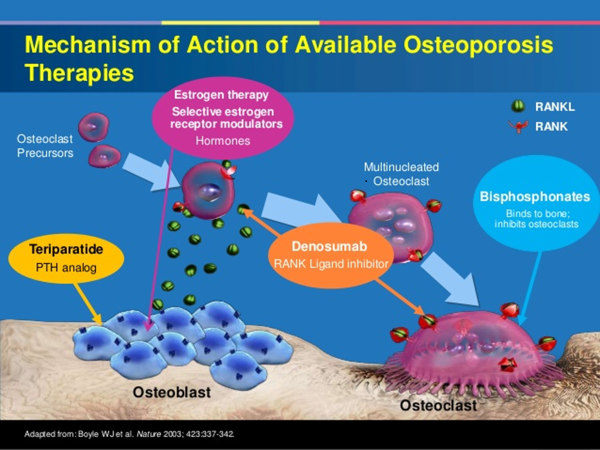
骨質疏鬆症藥物治療的機轉,這裡就不贅述了 ! 如果你還不了解骨質疏鬆藥,就先別唸這一篇了 !!!


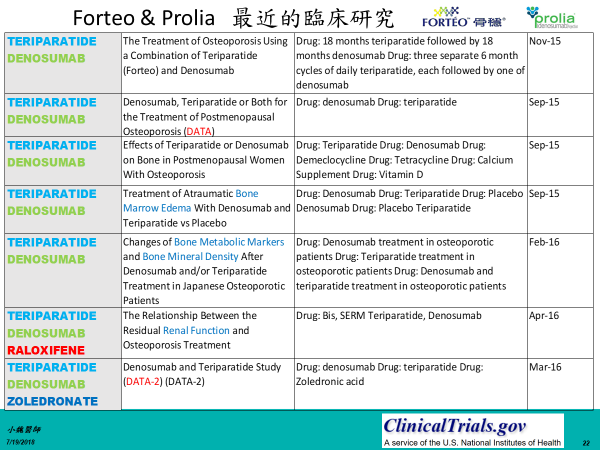
外科醫師,最討厭的就是唸書了,尤其是一大堆的Trials試驗,用一大堆的簡寫,讓人摸不著丈二金剛。
就簡單的說,現在骨質疏鬆症的治療藥物,從一開始的雙磷酸鹽類,常見的有Alendronate(Fosamax® / Fosamax® Plus D,福善美® ;Binosto®,骨密妥®)、Zoledronate(Aclasta®,骨力強®) 、Ibandronate(Bonviva®,骨維壯®)...等,主要是抑制蝕骨細胞、降低骨質流失,達到減少骨折機會的功效。
慢慢找到適合女性的Raloxifene (Evista®,鈣穩®)是一種選擇性雌激素接受器調節劑(SERM),針對骨骼也具有抗分解代謝的作用。鈣穩®之所以稱為「選擇性雌激素感受器調節劑」是因為其化學結構經過實驗室設計而成,因此有時也會被稱為「專門設計的雌激素」,屬於合成化合物,可以仿效雌激素的某些效益,同時免除某些副作用。鈣穩®減緩骨質流失的程度與雌激素差不多,核准用來治療及預防罹患骨質疏鬆症女性的骨折發生。是所有治療藥物當中,唯一被核准用於「預防」的藥物。
2011年最新上市用於治療骨質疏鬆症的單株抗體藥物,是新一代走不同路徑的骨質疏鬆症治療藥物。Denosumab(Prolia®,保骼麗®)是一個對RANKL具專一性、高親和力結合的完全人類單株IgG抗體,可抑制破骨細胞的分化、活化、生存和抑制後續的骨吸收,治療有高骨折風險之停經後婦女骨質疏鬆症。在一隨機分派雙盲安慰劑對照的試驗中(FREEDOM trial),針對停經後婦女併有低骨密度的病患,在接受保骼麗®治療36個月後,可顯著降低新脊椎及髖部骨折的發生率。
上面三類都是破骨抑制的藥物。另一類治療藥物是造骨促進的藥物,Teriparatide(Forteo®,骨穩®)是合成的副甲狀腺素。於骨頭的作用是合成代謝,是目前唯一可以刺激骨頭合成(Bone Formation)的藥物。缺點是必須每日注射20mcg,而且價格昂貴。
所以,當Denosumab(Prolia®,保骼麗®)上市之後,想要越級打怪(上市前研究主要打雙磷酸鹽類藥物)。於是設計了一系列的頭對頭(head-to-head)的臨床研究,直接針對Teriparatide(Forteo®,骨穩®)設計了一系列的研究。這一系列稱作DATA ( Denosumab and Teriparatide Administration ) 的研究,包含DATA、DATA extend、DATA-switch及最新的DATA-2。這裡就先不詳述,另開專題放在階段性用藥來說。市場上的恩怨情仇,聰明的醫生我們就隔山看虎鬥。

Forteo®,骨穩® 被打久了,也不是都沒感覺。雖然通過組織形態學和骨轉換標記(BTM)評估將denosumab定位為破骨抑制藥物。但是Prolia®一些研究報導,在給予denosumab後1-3個月內體內會有iPTH水平增加 (Bekker PJ 2004, McClung MR 2006, Seeman E 2011, Anastasilakis AD 2013, Makras P 2013, Sugimoto T 2015)。
有人提出PTH的升高,可能是 (促進生長) 抑制破骨細胞活動期間間接刺激骨形成所導致 (Seeman E 2011, Seeman E 2012),並與 (抑制破壞) denosumab誘導的皮質孔隙度降低相結合 (Reid IR 2010, Seeman E 2011, Seeman E 2012, Zebaze RM 2014),結果 (=) denosumab的長期骨密度(BMD)增加 (Papapoulos S 2015)。
當然Forteo®就不開心啦,世界上只有我骨穩®可以說有促進骨頭生長的作用(造骨促進),你Prolia®是另一類的(破骨抑制),不要越級打混仗,說你有促進骨質生長的功能,皇上不給的,你不能要。
於是就請了Dempster這位內分泌及組織學專家,設計了這個AVA phase 4的研究,並且刊登在JCEM (IF: 5.531)(Dempster DW 2016 )。

主要的目的,就是用直接採檢(Biopsy,最能直接確認骨質變化的方式)來確認促進骨質生長的功效。實驗方式如下圖
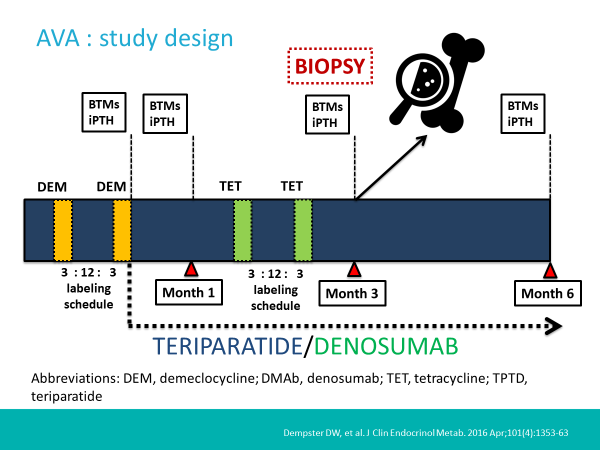
主要的目的,就是用直接採檢(Biopsy,最能直接確認骨質變化的方式)來確認促進骨質生長的功效。實驗方式如下圖
直接看結果 :
- iPTH的上升與促進骨生長無關
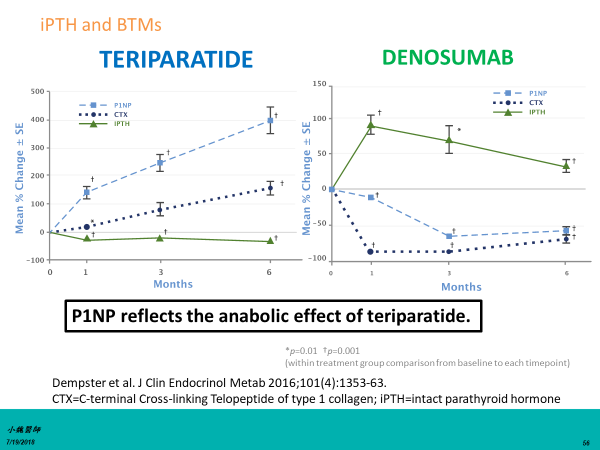
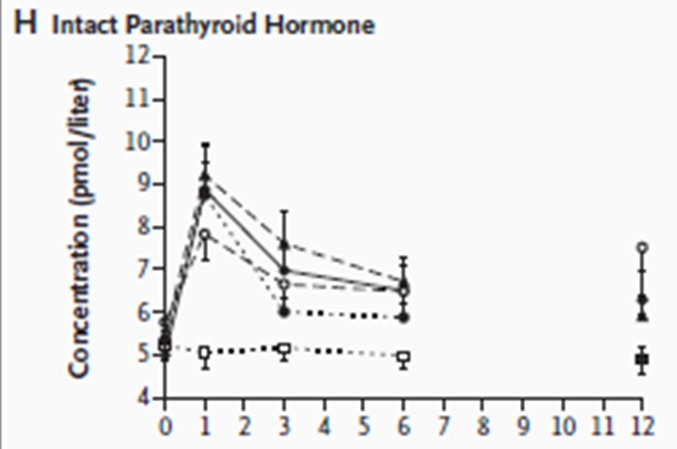
Forteo®在治療期間,iPTH是下降的。Prolia®相反,iPTH是上升的。
事實上發現,Forteo®在治療期間,iPTH注射後一小時,下降20%。這種效應是預期的,可能是因為Forteo®介導的對副甲狀腺內源性PTH釋放的抑制。
破骨抑制藥物治療第一個月,體內iPTH都是上升的。我們在研究中觀察到的PTH的增加並不是denosumab獨有的,並且可能是破骨抑制藥物類別的一個屬性,因為iPTH也隨著alendronate和zoledronic acid治療而增加。
PTH增加可能是維持血清鈣水平的代償性反應,體內血鈣會隨著抗吸收治療而降低。
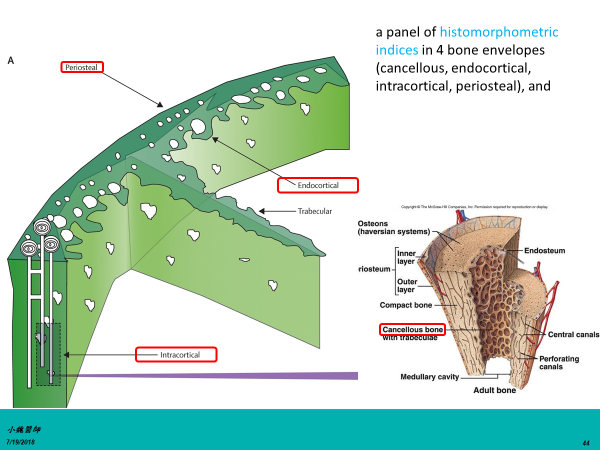
- 組織學證據

直接證明,經過Forteo®治療,MS/BS(礦化表面積/骨表面積)增加近19%而Prolia®治療,只增加1~1.5%,根本就沒有增加骨生成。
小魏醫師總結,雖然前面說是Prolia®越級打怪,其實Forteo®在之前就有類似的研究,叫做SHOTZ trial (Skeletal Histomorphometry in Subjects On Teriparatide or Zoledronic Acid Therapy),是跟雙磷酸鹽類 (Zoledronate,Aclasta®,骨力強®)相比較用直接穿刺採檢證實它的骨生成作用(Dempster DW 2018 )。有興趣的人可以拿出來比較看看。
結論只有一個,造骨促進藥物,現在還是只有一個,Teriparatide。
【參考資料】
Anastasilakis AD, P. S., Gkiomisi A, Bisbinas I, Gerou S, Makras P, (2013). "Comparativeeffectofzoledronicacidversusdenosumab on serum sclerostin and dickkopf-1 levels of naive postmenopausal women with low bone mass: a randomized, head-to-head clinical trial." J Clin Endocrinol Metab 98: 3206–3212.
Bekker PJ, H. D., Rasmussen AS, et al. (2004). "A single-dose placebo-controlled study of AMG 162, a fully human monoclonal antibody to RANKL, in postmenopausal women." J Bone Miner Res 19: 1059–1066.
Dempster DW, Z. H., Recker RR, Brown JP, Recknor CP, Lewiecki EM, Miller PD, Rao SD, Kendler DL, Lindsay R, Krege JH, Alam J, Taylor KA, Janos B, Ruff VA, (2016 ). "Differential Effects of Teriparatide and Denosumab on Intact PTH and Bone Formation Indices: AVA Osteoporosis Study." J Clin Endocrinol Metab 101(4): 1353-1363.
Dempster DW, Z. H., Ruff VA, Melby TE, Alam J, Taylor KA, (2018 ). "Longitudinal Effects of Teriparatide or Zoledronic Acid on Bone Modeling- and Remodeling-Based Formation in the SHOTZ Study." J Bone Miner Res 33(4): 627-633.
Makras P, P. S., Papatheodorou A,Kokkoris P,Chatzifotiadis D, Anastasilakis AD, (2013). "Parathyroid hormone changes following denosumabtreatmentinpostmenopausalosteoporosis." ClinEndocrinol (Oxf) 79: 499–503.
McClung MR, L. E., Cohen SB, et al . AMG162BoneLoss Study Group. (2006). "Denosumab in postmenopausal women with low bone mineral density." N Engl J Med 354: 821–831.
Papapoulos S, L. K., Roux C, et al. (2015). "The effect of 8 or 5 years of denosumab treatment in postmenopausal women with osteoporosis: results from theFREEDOMExtension study." Osteoporos Int 26: 2773–2783.
Reid IR, M. P., Brown JP, et al. (2010). "Denosumab Phase 3 Bone Histology Study Group. Effects of denosumab on bone histomorphometry: the FREEDOM and STAND studies." J Bone Miner Res 25: 2256–2265.
Seeman E, L. C., Austin M, et al. (2011). "The transitory increase in PTH following denosumab administration is associated with reduced intracortical porosity: a distinctive attribute of denosumab therapy." J Bone Miner Res 26(Suppl1): presentation1064.
Seeman E, L. C., Austin M, et al. (2012). "Association between transitory increase in PTH following denosumab administration and reduced intracortical porosity is a distinctive attribute of denosumab therapy." Bone 50: S162.
Sugimoto T, M. T., Hosoi T, et al. (2015). "Three-year denosumab treatment in postmenopausal Japanese women and men with osteoporosis: results from a 1-year open-label extension of the DenosumabFractureInterventionRandomizedPlaceboControlledTrial (DIRECT)." Osteoporos Int 26: 765–774.
Zebaze RM, L. C., Austin M, et al. (2014). "Differing effects of denosumab and alendronate on cortical and trabecular bone." Bone 59(173–179).