【骨鬆Q&A 019】什麼是FREEDOM (Fracture REduction Evaluation of Denosumab in Osteoporosis Every 6 Months) tr
【骨鬆Q&A 015】跟大家說明了Prolia®的臨床三期研究有DEFEND(Prevention Study)、FREEDOM、DECIDE、STAND與post-hoc(Transition Study)trails。
現在回頭來看看Prolia®上市所依據的臨床三期研究,有兩大部分。
- 一個部分是與雙磷酸鹽類的間接(因為是針劑對口服劑)頭對頭比較,包含【骨鬆Q&A 016】DECIDE、STAND trails,只有比較BMD。
- 一個部分是臨床三期綜合性研究,就是【骨鬆Q&A 019】FREEDOM trials。

FREEDOM包含綜合性的內容,討論用藥三年的BMD、BTM、fracture risk、high risk sub-analysis、discontinuation等等 (Cummings SR 2009)。
之後也延續滿八年,發表在ASBMR的oral presentation (Bilezikian JP 2014),最終設定在滿十年 (Bone 2016)。
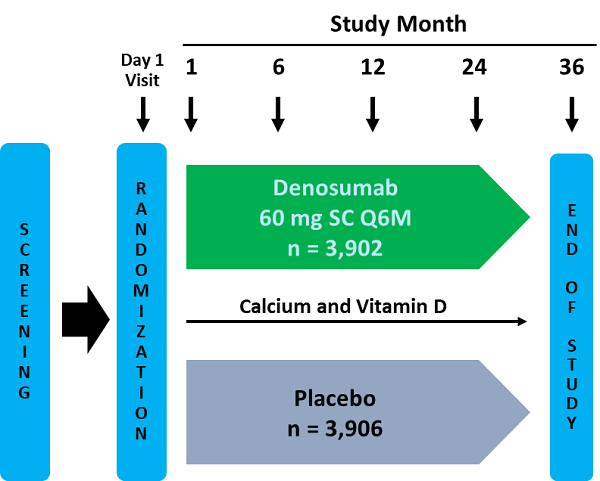
一項為期3年的國際隨機安慰劑對照研究,納入了7,808名停經後婦女。
1.骨折率
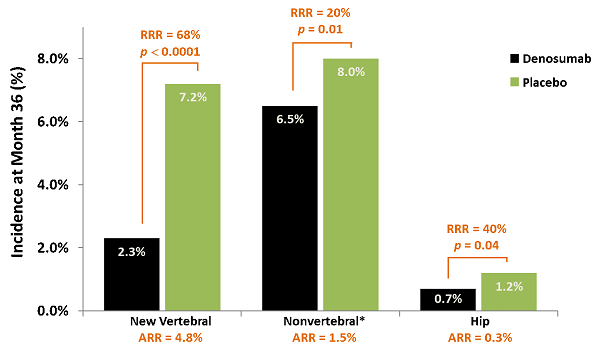
在主要終點分析中,DMab與安慰劑組相比,新形成椎體骨折的相對危險度為0.32,相對減少68%(p = 0.0001),絕對減少4.8%。
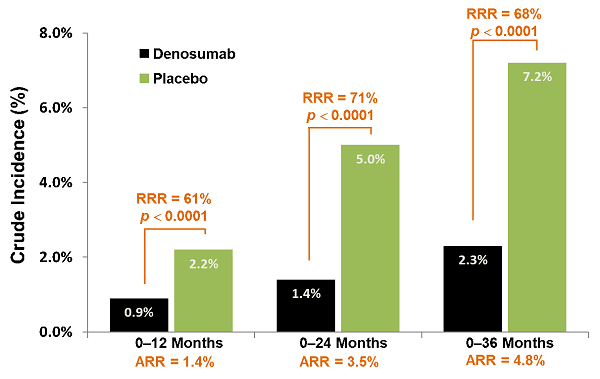
試驗12個月,24個月和36個月相對危險度相似,分別為61%,71%和68%。
在研究的第36個月,每6個月用60mg的DMab治療顯著降低了新椎體骨折68%的風險。
2.BMD 骨質密度
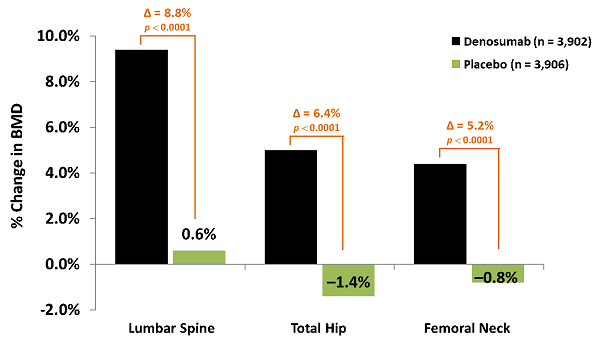
3年後,DMab與安慰劑相比在腰椎上的BMD顯著上升8.8%(95%CI,8.6-9.1),全髖6.4%(95%CI,6.2-6.6),5.2%(95%CI,5.0 -5.4)。
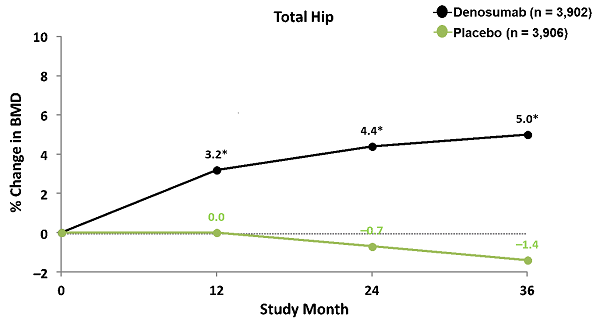
通過3年的治療,DMab髖部BMD與安慰劑相比持續增加。
3年後,與安慰劑組相比,DMab在全髖關節骨密度增加了6.4%(95%CI,6.2-6.6)。
3.BTM 骨代謝標誌
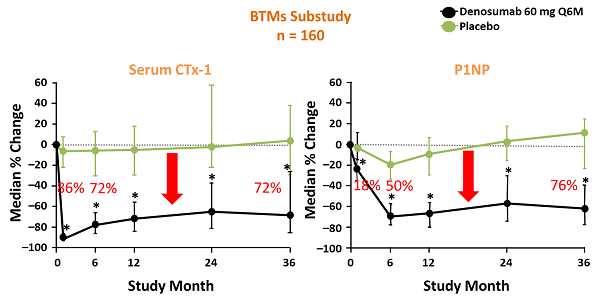
在第一次注射前,1個月後以及在6個月,12個月,24個月和36個月的注射前,使用160名患者使用空腹血清樣本進行BTMs評估骨吸收標誌物(CTx-1),骨形成的標誌物(P1NP)的結果。
CTx-1的結果:
在第1月,DMab將CTx-1水平降低86%。
在第6個月,DMab將CTx-1水平降低了72%。
在第36個月,DMab將CTx-1水平與安慰劑相比降低了72%。
P1NP的結果,骨形成的標誌物:
在第1個月,DMab將P1NP水平降低18%。
在第6個月,DMab將P1NP水平與安慰劑相比降低了50%。
在第36個月,DMab對安慰劑組的P1NP水平降低了76%。
4.BMD DXA亞組
原本的研究以髖部BMD為大宗,另分亞組作其他部位BMD的比較 (Bolognese MA 2013)。
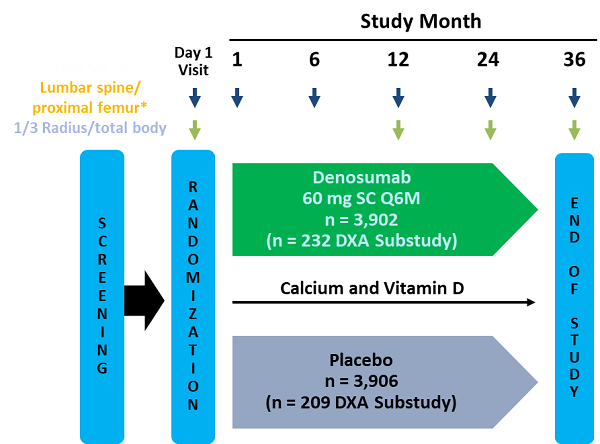
在DXA亞組中的441名患者佔所有參加第三階段試驗的患者的34%。
DXA子研究的數據來自213個研究中心中的19個研究中心,其中BMD被更頻繁地評估,並在額外的骨骼部位進行評估(Lunar、Hologic都有)。

全組腰椎平均百分比變化為8.8%(95%CI 8.6%,9.1%,p <0.0001)。
全組總髖關節平均百分比變化為6.4%(95%CI 6.2%,6.6%,p <0.0001)。
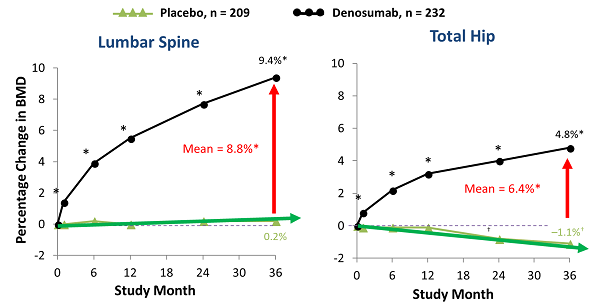
股骨頸平均百分比變化為5.2%(95%CI 5.0%-5.4%,p <0.0001)。
轉子平均百分比變化為8.3%(95%CI 8.0%-8.6%,p <0.0001)。
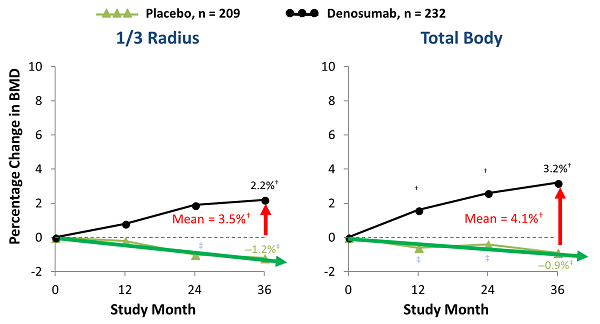
用DMab治療觀察到的骨密度增加在所有部位均有進展性和顯著性,除1個月股骨頸評估外,所有時間點均得到評估。
5.橈骨BMD,骨強度和手腕骨折
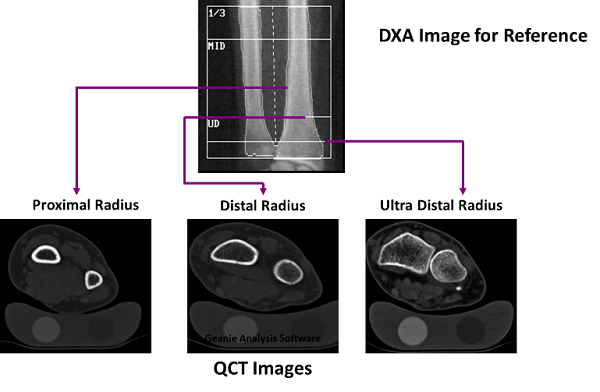
雙能X射線吸收測定法(DXA)測量面骨骨礦物質密度(aBMD),並提供有限的骨幾何評估能力。
定量計算機斷層掃描(QCT)通過三維測量體積BMD(vBMD)來補充DXA。
此外,QCT測量可用於通過確定估計物體抵抗扭轉和彎曲的能力的極坐標慣性矩(PMI,polar moment of inertia)來評估功能骨骼強度 (Simon JA 2013)。
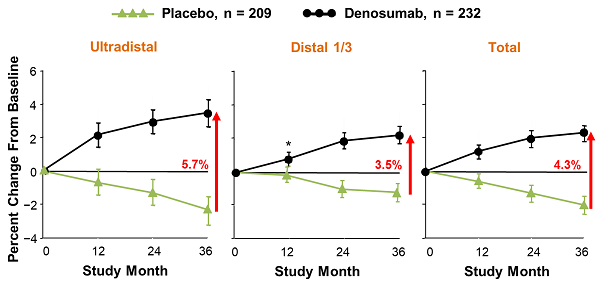
觀察到用DXA評估的BMD的顯著增加(p <0.01)。
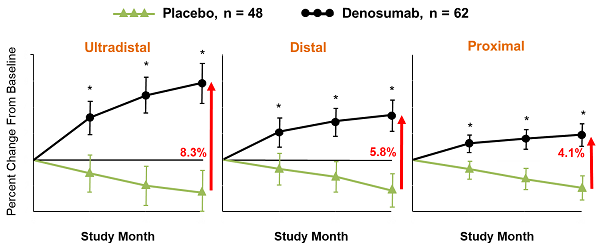
觀察到用QCT評估的vBMD顯著增加(p <0.05)。
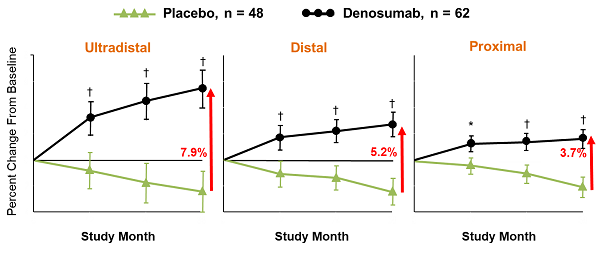
在所有橈骨部位,BMC顯著增加(p <0.05)。

BMD和BMC在橈骨的改善,與骨骼強度測量的PMI顯著增加相關聯(p <0.05)。

BMD > -2.5,用DMab治療的女性手腕骨折發生率與未接受治療的女性相似。BMD ≦ -2.5的女性中,DMab觀察到手腕骨折顯著降低40%。
但在整個關鍵階段3試驗中,DMab觀察到的手腕骨折減少無統計學意義。
6.高骨折風險病人
-
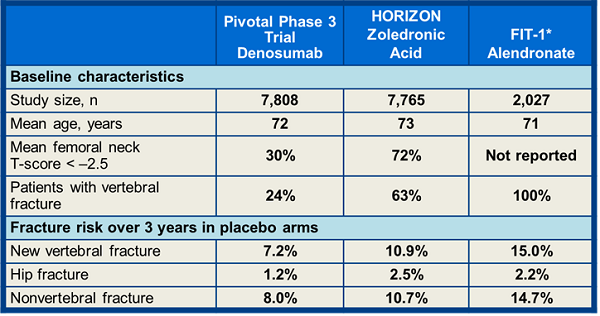
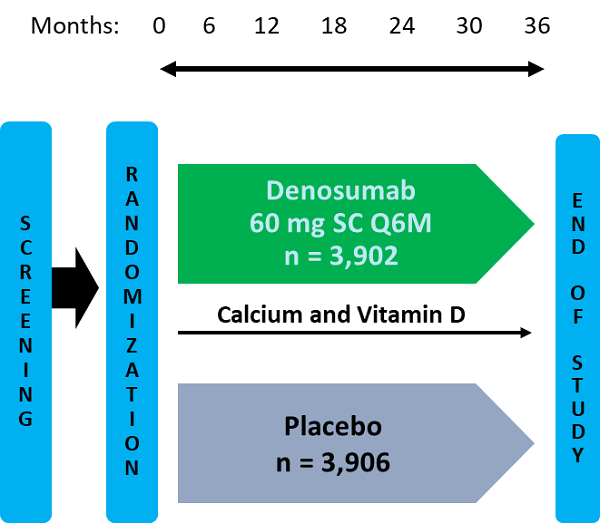
Pivotal (Cummings SR 2009)3期試驗是每6個月接受denosumab或安慰劑SC注射的絕經後婦女3年研究。
- 椎骨骨折事件定義為: 在基線正常的椎體中≥1級的增加。
- 排除以下非椎骨骨折:顱骨骨折,面部,下頜骨,掌骨,手指或腳趾,病理性骨折和與嚴重創傷相關的骨折。
-
HORIZON (Black DM 2007)是接受了每年zoledronic acid 或安慰劑輸注的絕經後婦女的3年研究
- 形態學的椎體骨折事件定義 : 為通過定量形態測定術椎體降低高度≥20%和4mm。
- 對於非椎骨骨折,排除以下情況:腳趾,面骨和手指骨折以及由過度創傷造成的骨折。
-
FIT-1 (Black DM 1996)是一項為期3年的絕經後婦女接受alendronate或安慰劑的研究
- 椎骨骨折事件定義為距離基線X線片的任何椎體高度減少20%和≥4mm。
- 以下骨折被排除:病理性骨折(例如惡性疾病),由於過度創傷引起的骨折,以及面部和顱骨的骨折。
根據安慰劑組的骨折率,Pivotal 3期試驗中骨質疏鬆症患者的骨折風險低於HORIZON或FIT-1的骨折風險 (Boonen S 2011)。
該分析的目的是評估在較高骨折風險的第三階段試驗受試者亞組中,DMab對新骨折發生率的降低 (Boonen S 2011)。
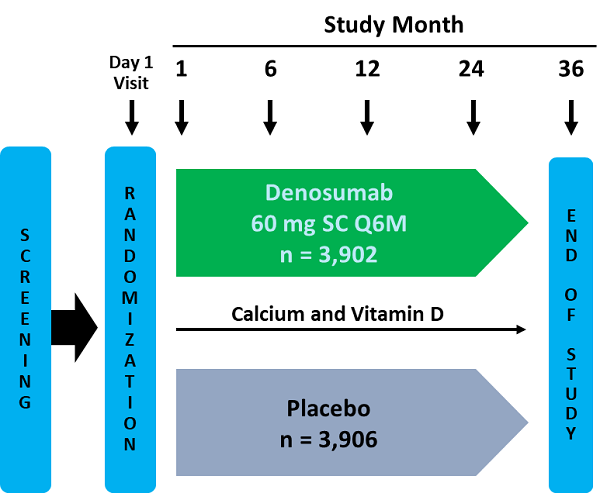
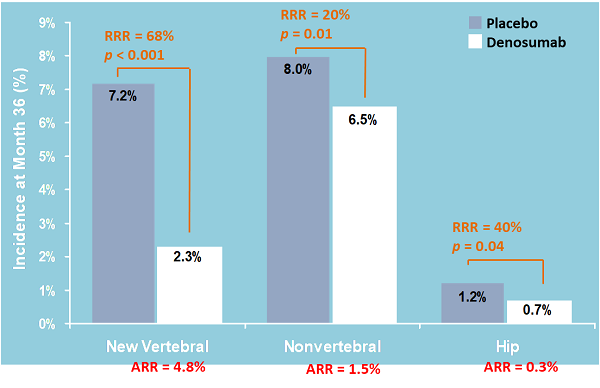
新椎體骨折的相對危險度為0.32減少68%。
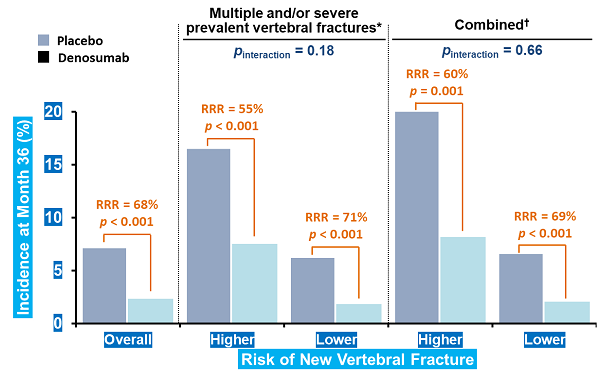
在Pivotal 3期試驗中的總體試驗人群中,DMab組36個月新發椎體骨折發生率為2.3%,安慰劑組為7.2%(風險比為0.32,風險比為95%CI = 0.26〜 0.41,p <0.001)
在具有中度或重度畸形≥2次的常規椎體骨折≥2%的高危患者的亞臨床分析中(Pivotal 3期試驗人群的10%左右);高風險安慰劑組n = 343;更高風險的denosumab n = 359),DMab將新椎體骨折的風險從16.6%降低到7.5%(9.2%的絕對風險下降,55%的相對風險降低,95%CI相對風險降低= 31%至71% ,p <0.001)
在具有股骨頸多發和/或中度或重度椎體畸形的高風險患者子集的事後分析中,BMD T評分≤2.5(約佔Pivotal 3期試驗人群的5%);高風險安慰劑n = 154;更高風險DMab n = 172),DMab將新的椎骨骨折風險從20.1%降至8.1%(絕對風險降低12.3%,相對風險降低60%,相對風險降低95%CI = 28% 78%,p = 0.001)
該次分析的p相互作用無統計學意義
相互作用(或異質性)的檢驗是隨機試驗中亞組治療效果的比較。換句話說,為了進行相互作用的測試而提出的問題可能是:“觀察到的結果是否在子組之間是一致的”? 還是“觀察到的效果是否被另一個變量修改”?本次分析中排除了高創傷和病理性骨折 (Altman DG 1996, Altman DG 2003)
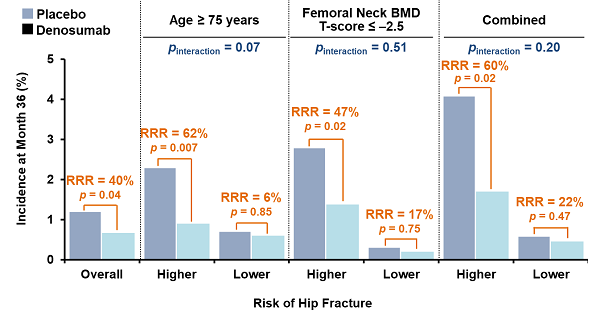
反映了每個高風險亞組髖部骨折累積發生率的Kaplan-Meier估計。
7.停藥後的變化
該分析的目的是通過評估停用治療的關鍵3期試驗中的患者,了解DMab治療停藥後骨質疏鬆症患者的骨折發生率 (Brown JP 2013)。
回顧性分析包括在接受2-5劑(安慰劑組或安慰劑組)劑後停止治療的患者,持續研究參與≥7個月(自上次劑量+ 1個月訪視窗口≥6個月) 0.1
最大治療觀察期可能為24個月。
在關鍵階段3試驗的治療期間,安慰劑組與DMab組有更多的患者發生骨折(安慰劑組為19%,DMab組為11%),BMD顯著降低(17% 對於安慰劑,對於DMab為1%)。
更多的患者由於DMab組的惡性腫瘤(安慰劑組為4%,DMab為9%),因此停止了研究。
乳腺癌是最常見的惡性腫瘤類型,導致停藥(0.7%為安慰劑,0.9%為DMab)。
在治療期間,安慰劑組與DMab組的更多患者在最後一次給藥DMab後開始其他治療(安慰劑組為42%,DMab為28%)。
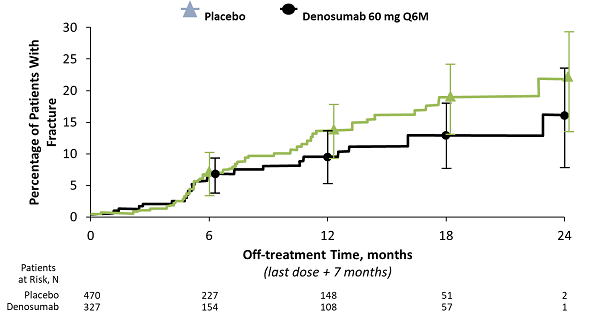
治療期間頭6個月,治療組間骨折率相似
在治療後6個月內,觀察到安慰劑組的骨折率較高,但與24小時觀察期間的DMab組相比差異無統計學意義。
小魏醫師總結,FREEDOM是臨床三期綜合性研究,研究及後續分析包含
- 一般BMD、BTM、fracture risk、
- 亞組BMD
- 亞組高危病患骨折率
- 停藥後的變化
重點除了強調可以減少臨床新發生椎體骨折68%,增加BMD、減少BTM、還分析高危病患也有功效及停藥後骨折率變化。其中改善骨折率佳的是椎體,改善BMD佳的是髖部。
不同於【骨鬆Q&A 014】Prolia®的第一、二期臨床研究中所提到的停藥後BMD急速下降及BTM過渡反彈,對於骨折率的影響是正面的,但臨床醫師還是得考量接續用藥的可能性,將停藥影像降到最小(如同【骨鬆Q&A 001】雙磷酸鹽的Drug Holiday)。
【參考資料】
- Altman DG, B. J. (2003). "Interactions revisited: the difference between 2 estimates." BMJ 326: 219.
- Altman DG, M. J. (1996). "Interaction 1: heterogeneity of effects." BMJ 313: 486.
- Bilezikian JP, B. C., Lin CJF, et al. (2014). "Denosumab restores cortical bone loss at the distal radius associated with aging and reduces wrist fracture risk: analyses from the FREEDOM extension cross-over group. ."
- Black DM, C. S., Karpf DB, Cauley JA, Thompson DE, Nevitt MC, (1996). "Randomised trial of effect of alendronate on risk of fracture in women with existing vertebral fractures. Fracture Intervention Trial Research Group." Lancet 348: 1535–1541.
- Black DM, D. P., Eastell R, (2007). "Once-yearly zoledronic acid for treatment of postmenopausal osteoporosis." N Engl J Med 356(18): 1809-1822.
- Bolognese MA, S. T. C., Zanchetta JR, et al. (2013). "Denosumab significantly increases DXA BMD at both trabecular and cortical sites: results from the FREEDOM study." J Clin Densitom 16: 147-153.
- Bone, H. G., et al. (2016). "Ten years of Denosumab (DMAB) treatment in postmenopausal women with osteoporosis. Results from the FREEDOM Extension trial." Osteoporosis International 27(Supplement 1): 135-136.
- Boonen S, A. J., Man Z, et al. (2011). "Treatment with denosumab reduces the incidence of new vertebral and hip fractures in postmenopausal women at high risk." J Clin Endocrin Metab 96: 1727-1736.
- Brown JP, R. C., Törring O, et al. (2013). "Discontinuation of denosumab and associated fracture incidence: analysis from the fracture reduction evaluation of denosumab in osteoporosis every 6 months (FREEDOM) trial." J Bone Miner Res 28: 746-752.
- Cummings SR, S. M. J., McClung MR, (2009). "Denosumab for prevention of fractures in postmenopausal women with osteoporosis." N Engl J Med 361(8): 756-765.
- Simon JA, R. C., Moffet AH Jr, et al. (2013). "Impact of denosumab on the peripheral skeleton of postmenopausal women with osteoporosis: bone density, mass, and strength of the radius, and wrist fracture." Menopause 20: 130-137.